Isaac Carrasco
LV, PhD, Acred. Dermatología AVEPA, GPCertDerm, PGDerm
AniCura Glòries
Imágenes cedidas por el autor
El sistema inmunitario (SI) es fundamental en la protección frente a patógenos y agresiones externas. Pero, en ocasiones, aquello que nos protege puede volverse en nuestra contra, dando lugar a procesos patológicos altamente complejos y difíciles de manejar, las enfermedades autoinmunitarias.
Para entender cómo funcionan estas enfermedades es de gran importancia conocer cómo funciona el SI. Históricamente lo dividimos en dos “compartimentos” teóricos independientes:
- Sistema inmunitario innato: actúa de una manera inmediata e inespecífica frente a agresiones potenciales.
- Sistema inmunitario adaptativo: responde de una manera específica y con memoria, normalmente tras la actuación previa del sistema inmunitario innato.
Siempre se ha considerado al sistema inmunitario innato como algo primitivo que actúa de manera poco específica gracias a las barreras epiteliales, determinadas moléculas segregadas con capacidad antimicrobiana inespecífica y la actividad de las células natural killers (NK). Pero en realidad no es del todo así, como veremos a continuación.
Un actor fundamental del sistema inmunitario innato son las células dendríticas (células presentadores de antígeno – CPA), que son las primeras en tener contacto con los patógenos (antígeno) al penetrar las barreras mucocutáneas. El contacto CPA-antígeno es parcialmente específico, y está mediado por la interacción entre patrones moleculares asociados a patógenos (PAMP) (del propio patógeno) y los receptores de reconocimiento de patrones (PRR) (del paciente).
La unión PAMP-PRR pone en marcha una señal intracelular específica que da lugar a la activación de genes de la CPA, fundamentales para la activación posterior de linfocitos T (sistema inmunitario adaptativo). Así, el tipo de activación que se produce en la CPA condiciona la manera en que el sistema inmunitario adaptativo va a responder al estímulo patógeno. Todos los linfocitos Th tienen un precursor común, Th0 (naïve), que se comportará de una manera u otra dependiendo de la información que reciba por parte de la CPA (esta producirá unas u otras citoquinas dependiendo a su vez del tipo de estímulo inicial) (tabla 1).
| SUBPOBLACIÓN | CITOQUINA MAYORITARIA | PAPEL EN LA RESPUESTA INMUNITARIA ADAPTATIVA |
|---|---|---|
| Th1 | IFN-g | Inmunidad celular |
| Th17 | IL-17 | Inflamación |
| Th2 | IL-4 | Inmunidad humoral |
| Th9 | IL-9 | Alergia |
| Treg | IL-10 | Supresión |
| Th3 | TGF-b | Tolerancia |
Una vez que se activa el sistema inmunitario adaptativo, sus funciones van a depender de muchas subclases de linfocitos T:
- La respuesta Th1 se caracteriza por producir, entre otras citoquinas, IFN-γ, que activa células fagocíticas (ej. macrófagos) o linfocitos citotóxicos, poniendo en marcha lo que se llama la inmunidad celular.
- La respuesta Th2 se caracteriza por producir un gran panel de citoquinas, entre ellas IL-4, IL-5, IL-9, e IL-13, que permiten que se activen linfocitos B, y que se conviertan a su vez en células plasmáticas encargadas de producir anticuerpos (inmunoglobulinas antígeno-específicas), dando lugar a lo que se conoce como la inmunidad humoral.
- Y además existen otras subclases de linfocitos T, como los Th17, que producen IL-17 (importante en la respuesta frente agentes infecciosos); o los Th9, que producen IL-9 (importante en reacciones alérgicas).
Todo esto permite que el sistema inmunitario sea altamente eficiente, en cuanto a la defensa frente a patógenos externos se refiere. Pero es fundamental que esa vigilancia inmunitaria no se vuelva en contra del propio individuo para que no se produzca un “auto-ataque” inmunitario. Por tanto, debe existir inmunotolerancia (auto tolerancia) frente a potenciales antígenos propios, situación que se pierde en las enfermedades autoinmunitarias, como iremos viendo.
Fundamentalmente, se pierde la función de los linfocitos T reguladores (Treg), con una presentación inadecuada de autoantígenos por parte de las CPA. Como consecuencia, el sistema inmunitario ataca dichos autoantígenos, y se activan principalmente linfocitos Th1 en aquellas enfermedades en las que existe una destrucción citotóxica de los tejidos diana; o linfocitos Th2, en aquellas enfermedades en las que esté implicada la formación de anticuerpos. Afortunadamente esta pérdida de la auto tolerancia es poco común, y solo el 1,5 % de los pacientes que acuden a servicios de referencia de dermatología presentan este tipo de patologías.
Las enfermedades en las que el sistema inmunitario actúa de manera inadecuada produciendo daños en la piel se pueden clasificar en dos grupos:
- Enfermedad autoinmunitaria como tal: el sistema inmunitario deja de tolerar algunas moléculas propias (se pierde la inmunotolerancia), y se inicia una respuesta inmunitaria inadecuada frente a estructuras normales del individuo. Como veremos a continuación, el aspecto clínico de las lesiones dependerá de la diana antigénica y de la gravedad de la respuesta inmunitaria que se produzca.
- Enfermedad inmunomediada: el antígeno frente al que actúa el sistema inmunitario no es propio (fármacos, bacterias, virus), pero pone en marcha una respuesta inmunitaria que daña los tejidos del paciente por diferentes mecanismos. Este grupo de situaciones clínicas queda fuera de las expectativas de este artículo.
Breve repaso de algunas de las dermatosis autoinmunitarias que afectan al perro y al gato
Pénfigo foliáceo
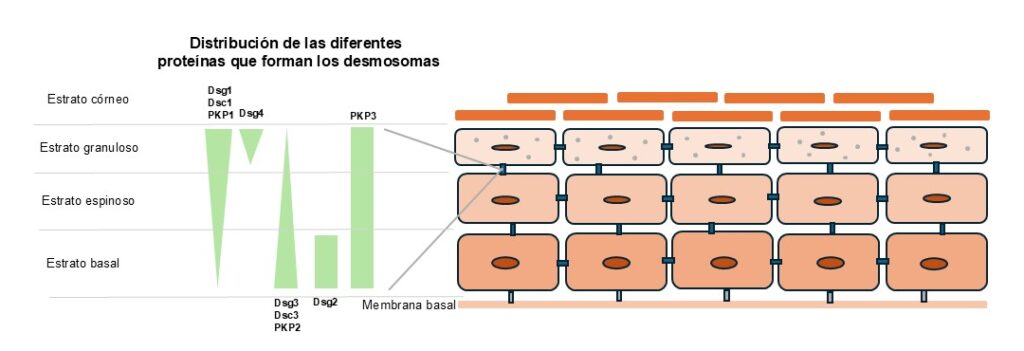
Es la enfermedad cutánea autoinmunitaria más común en la clínica diaria. Se produce por un ataque a algunas de las proteínas que componen los desmosomas, que son complejas estructuras que mantienen unidos a los queratinocitos entre sí. Dicho ataque da lugar a un proceso de separación o desprendimiento celular que recibe el nombre de acantolisis.
Como en muchas de las enfermedades autoinmunitarias en veterinaria, se desconoce parte de la fisiopatología del PF y, en la mayoría de los casos, la razón por la que el sistema inmunitario inicia la producción de anticuerpos contra las dos dianas terapéuticas principalmente implicadas en la enfermedad, la desmocolina 1 (Dsc1) y la desmogleína 1 (Dsg1). Se sospecha de una predisposición genética, ya que algunas razas están sobrerrepresentadas (como el Akita Inu o el Chow-Chow). Así mismo, en algunos estudios se ha asociado la aparición de la enfermedad a una historia dermatológica previa (principalmente, de dermatitis alérgica), sin que haya quedado claro si dicha asociación está relacionada con la propia enfermedad o con la gran cantidad de fármacos que reciben los pacientes alérgicos durante su vida. Del mismo modo que en medicina humana es bien sabido que el pénfigo puede ser inducido por fármacos, y también existen reportes en medicina veterinaria que avalan esta posibilidad.
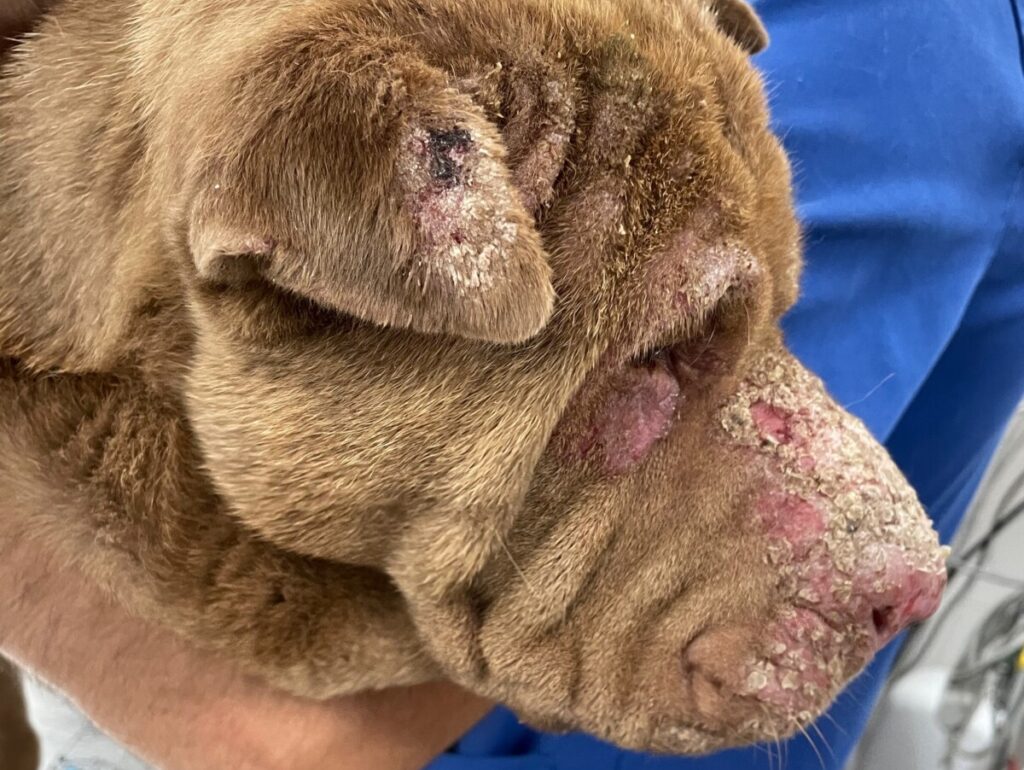
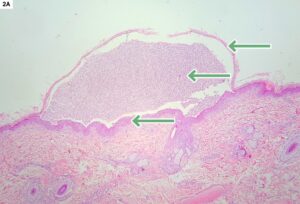
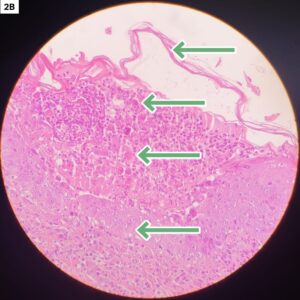
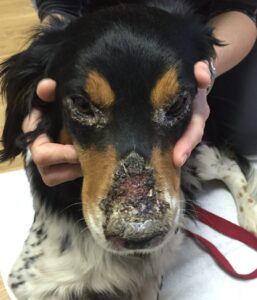
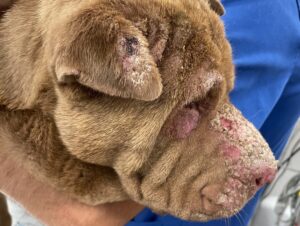
La Dsc1 y la Dsg1 son fundamentales para el buen funcionamiento de los desmosomas, principalmente en capas superficiales de la epidermis, por lo que las lesiones que se producen en los casos de PF serán superficiales (imagen 1). Es una enfermedad pustular en esencia (pústulas generalmente subcorneales, ya que se forman por debajo del estrato córneo de la epidermis (imagen 2), pero clínicamente solemos ver costras (que es la evolución natural de la pústula, ya que es una lesión muy friable).
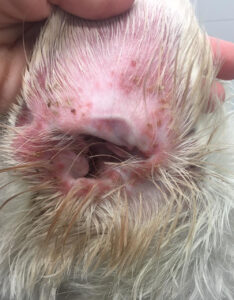
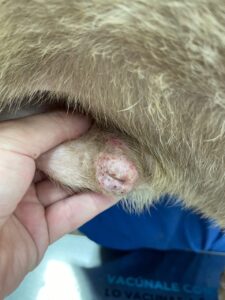
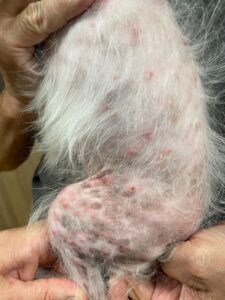
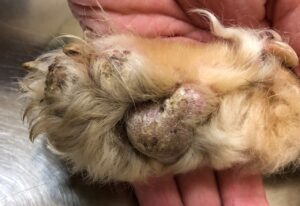
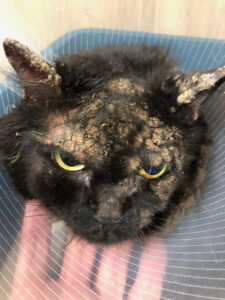
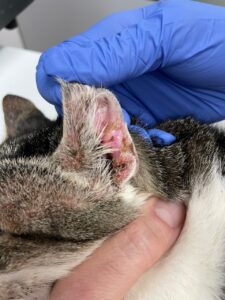
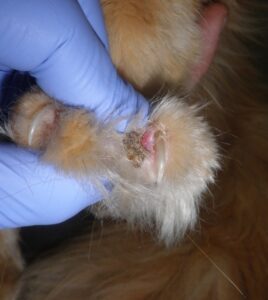
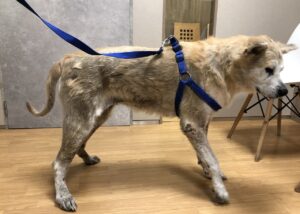
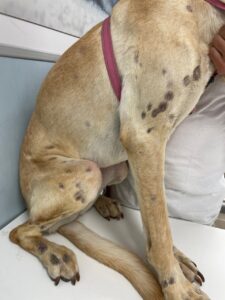
Suele verse afectada la cabeza, pero también otras zonas del cuerpo, (imagen 3). En el gato no es raro que se afecte la región periungueal, así como la piel que rodea los pezones (imagen 4). El grado de prurito es variable entre individuos, y aumenta en caso de que aparezcan infecciones secundarias.
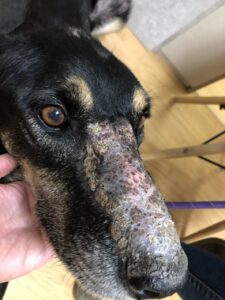
Imagen 3. Aspecto macroscópico de algunas lesiones dermatológicas en perros con pénfigo foliáceo.
Imagen 4. Aspecto macroscópico de algunas lesiones dermatológicas en gatos con pénfigo foliáceo. Imagen 4C cortesía de Marcos Fernández.
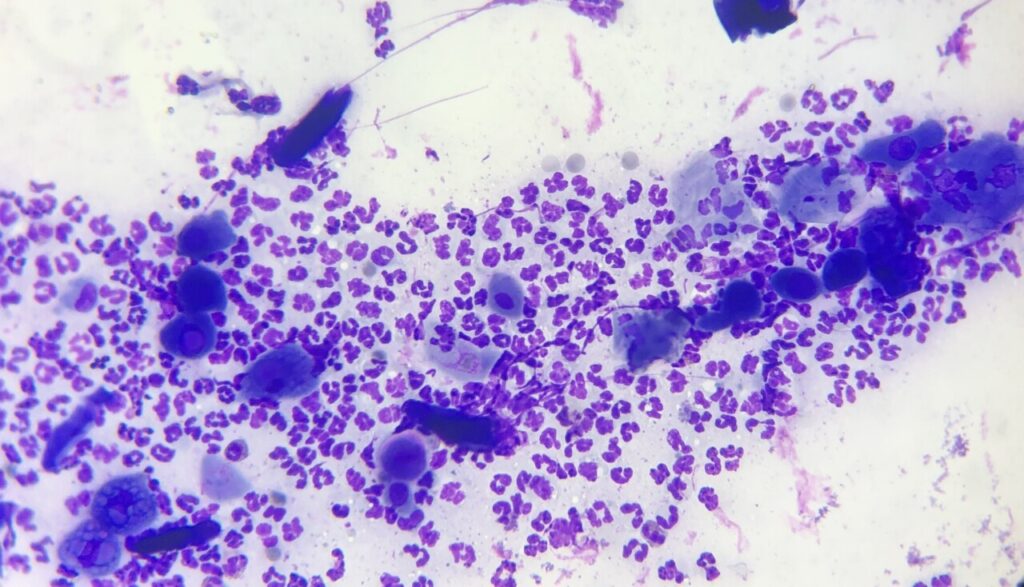
La falta de disposición de algunas de las pruebas de laboratorio que se utilizan en medicina humana hace que el diagnóstico de las dermatosis autoinmunitarias en veterinaria se base en el aspecto clínico, la historia clínica y el estudio histopatológico de las lesiones en muchos casos. Concretamente en los casos de PF, en la citología de las lesiones (idealmente pustulares) veremos una población variable de polimorfonucleares neutrófilos estériles y queratinocitos acantolíticos (imagen 5). A pesar de estos hallazgos citológicos y el aspecto clínico de las lesiones, para llegar al diagnóstico definitivo de PF es necesario realizar un estudio histopatológico de la piel, ya que existen otras enfermedades que pueden comportarse de una manera similar. Es fundamental descartar enfermedades infecciosas, como la leishmaniosis, antes de iniciar una terapia inmunosupresora en un paciente en el que sospechemos de PF.
Complejo lupus
El lupus es una enfermedad autoinmunitaria que puede afectar a diversos órganos a la vez o solo a la piel, desencadenada generalmente por factores ambientales y con una predisposición individual. Las lesiones cutáneas producidas por el lupus pueden ser directamente atribuidas a la enfermedad (por un ataque citotóxico contra los queratinocitos como, por ejemplo, en los casos del “lupus discoide”) o por cambios sistémicos que producen patología cutánea no específica (como los casos de vasculitis en el lupus eritematoso sistémico). Así, hace algunos años se propuso una nueva clasificación para los casos de lupus (imagen 6).

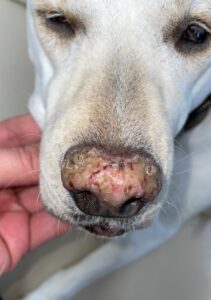
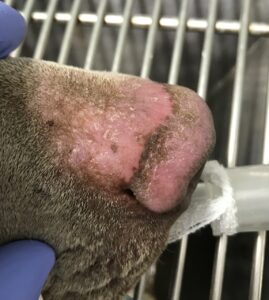
La forma más común en la clínica dermatológica diaria es el lupus eritematoso cutáneo, discoide. Existe una forma localizada (principalmente nasal) y una forma generalizada. Los signos clínicos clásicos son: despigmentación de la nariz, pérdida del “adoquinado” (dermatoglifos), eritema y descamación, y úlceras y costras en casos más crónicos (imagen 7). Las lesiones suelen empezar en la unión plano nasal/piel con pelo, o ventro-medial a las alas nariz. Es una patología que empeora con el daño solar, por lo que también puede afectar a otras zonas expuestas al sol, como orejas y párpados.
Imagen 7. Aspecto macroscópico de las lesiones observadas en perros con lupus eritematoso cutáneo nasal.
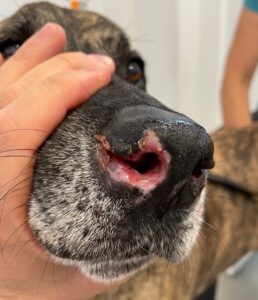
Como en la mayor parte de las enfermedades autoinmunitarias de la piel, el estudio histopatológico permitirá emitir un diagnóstico en la mayoría de los casos, descartando patologías que puedan cursar con un cuadro similar como la leishmaniosis o el síndrome úveo-dermatológico (imagen 8).
Imagen 8. A-C) Pacientes con leishmaniosis que afecta a la trufa. Nótese que las lesiones observadas pueden ir desde despigmentación difusa y dermatosis descamativa leve, hasta lesiones ulcerativas más graves. D) Paciente con síndrome uveodermatológico y afección de la piel de la trufa.
Adenitis sebácea
Hablamos de adenitis sebácea granulomatosa idiopática en aquellos casos en los que se produce un ataque inflamatorio/inmunitario contra las glándulas sebáceas, que acaba con su destrucción. Es posible que, entre otros, existan anomalías en el metabolismo y almacenaje de lípidos y defectos primarios de queratinización que obstruyen los conductos dando lugar a una inflamación glandular. En algunos artículos se ha reportado la aparición de adenitis después de una situación de estrés fisiológico (enfermedad, anestesia, cirugía). En cualquier caso, se sospecha de una predisposición genética, ya que existen razas sobrerrepresentadas, como el Akita Inu y el Caniche.
Las funciones de las glándulas sebáceas son múltiples. Las sustancias que producen lubrican la piel y el pelo, y ayudan al mantenimiento de la hidratación cutánea, colaborando así en la barrera física, química e incluso inmunológica de la piel.
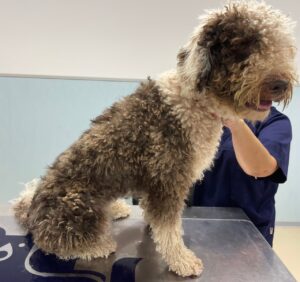
Por tanto, los signos clínicos más comunes en los casos de adenitis están relacionados con la pérdida de la funcionalidad y calidad de la secreción glandular, y podremos observar diferentes patrones clínicos dependiendo de la raza. Es común observar descamación, seborrea, cilindros foliculares y eritema leve en razas como el Akita Inu (imagen 9); cambios en el color del pelo o pérdida del rizo característico en razas como el perro de aguas o el Caniche (imagen 10); o alopecia multifocal con descamación variable en algunas razas de pelo corto (imagen 11). No es raro que se acompañe de otitis externa, y el prurito aparece cuando se producen infecciones secundarias (muy común, casi en la mitad de los pacientes afectados).
Imagen 9. Adenitis sebácea en Akita Inu. Nótese el mal aspecto general del manto, con alopecia difusa y seborrea, que afecta también a pabellones auriculares y cabeza.
Imagen 10. Adenitis sebácea en perro de aguas. Nótese el cambio en la calidad, cantidad y aspecto del manto, que pierde su rizo característico.
Imagen 11. Adenitis sebácea en dos perros de pelo corto, que cursa con alopecia multifocal.
El diagnóstico de la adenitis sebácea pasa por realizar un estudio histopatológico de la piel, donde observaremos el ataque inflamatorio dirigido a la glándula, o la desaparición total de la misma (dependiendo de la cronicidad del cuadro). Es importante descartar la implicación de la leishmaniosis en el cuadro clínico, mediante el uso de tinciones específicas en la muestra de biopsia.
Alopecia areata
Los folículos, desde que se forman en la fase embrionaria, se encuentran en transformación cíclica durante toda la vida del individuo, gracias a la acción de la gran cantidad de células precursoras de queratinocitos y melanocitos que existen a nivel de bulbo. Estas células gozan de un privilegio inmunológico que las protege de ataques inmunitarios, ya que durante la fase de formación del pelo y de la melanogénesis se producen muchas moléculas potencialmente antigénicas.
Cuando este privilegio inmunológico se pierde (por factores genéticos y/o ambientales) se produce un ataque inmunitario contra el folículo en anagén, interrumpiéndose así el ciclo folicular, dando lugar a un cuadro de alopecia areata. En este caso sí que se trata de una enfermedad autoinmunitaria órgano-específica, ya que afecta al folículo casi exclusivamente (aunque se ha descrito la afección de las uñas y del epitelio pigmentario de la retina).
Es común observar alopecia no inflamatoria, que suele afectar a la cabeza, aunque también puede llegar a comprometer a la totalidad de la superficie corporal (imagen 12). La alopecia que se produce es potencialmente reversible, ya que no se afectan células precursoras; y no es raro que cuando el pelo recrece sea de color blanco (leucotriquia), por el ataque que se ha producido contra células pigmentadas.
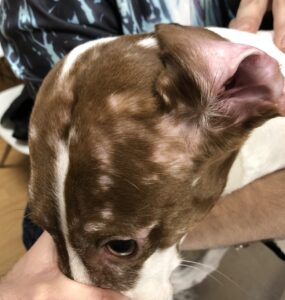
El diagnóstico definitivo se consigue por exclusión de otras patologías que produzcan alopecia y mediante el estudio histopatológico de la piel.
Conclusiones
Las patologías autoinmunitarias se producen por una pérdida de la auto tolerancia frente a algunas moléculas propias del individuo, dando lugar a cuadros dermatológicos muy diversos según la diana antigénica y la intensidad de la respuesta inmunitaria. Conseguir un diagnóstico adecuado pasa por realizar un estudio histopatológico de la piel, y es fundamental descartar otras patologías que puedan tener un curso clínico similar. En ocasiones puede resultar un desafío diagnóstico, por lo que debemos trabajar con dermatopatólogos experimentados en este tipo de enfermedades.
Bibliografía recomendada: