Alejandro Sánchez López
Servicio de Anestesia y Analgesia del Hospital Veterinario Puchol
La anestesia es una especialidad que ha ido cobrando mayor relevancia en las últimas décadas en pequeños animales1. Por ello, cada vez es más habitual que, tanto los tutores como los profesionales, decidan realizar procedimientos que requieren anestesia general en pacientes con patologías cardiovasculares complejas en los que hace tiempo dicha anestesia se hubiera evitado.
Cada enfermedad cardiovascular tiene unas características propias y, por ello, a la hora de abordar la anestesia de un paciente cardiópata, es necesario conocer la fisiopatología específica de cada una de ellas, así como su gravedad2.
El defecto del septo interventricular (DSIV) es aproximadamente la quinta malformación cardiaca congénita más frecuente en perros3. Se produce como consecuencia de una fusión incompleta del septo interventricular durante la embriogénesis4, lo que lleva a un flujo de sangre del ventrículo izquierdo al derecho durante la sístole4,5. Puede aparecer de forma aislada, aunque a menudo se presenta junto con otras patologías congénitas como estenosis pulmonar, estenosis aórtica o conducto arterioso persistente3,4. Aunque no se ha identificado una predisposición racial como tal, algunos estudios muestran una mayor incidencia de presentación en pinscher, bulldog francés y pastor alemán5.
Los DSIV de pequeño tamaño no suelen producir consecuencias clínicas importantes y a menudo los pacientes solo presentan un soplo cardiaco de bajo grado3-5. En caso de DSIV más grandes y/o con otras enfermedades cardiacas concurrentes, el pronóstico es más grave, principalmente si se produce una reversión del flujo sanguíneo a derecha-izquierda4,5.
El objetivo de este trabajo es describir el manejo anestésico en un perro con DSIV grave con otras patologías cardiacas asociadas, para la amputación de dos falanges necrosadas.
Descripción del caso
Se presentó en consulta un perro mestizo, macho entero de 5 años y 13,7 kg, para su evaluación por parte del Servicio de Cirugía. El paciente presentaba una lesión en la extremidad anterior derecha (EAD), presuntamente como consecuencia de un traumatismo que gradualmente había producido la necrosis de los dedos II y III. Se tomó un cultivo de la lesión, que reveló la existencia de Pseudomonas putida sensible a la amikacina.
Por otro lado, al paciente, cuando era cachorro, se le diagnosticó un DSIV con insuficiencia aórtica y mitrálica asociada y grave dilatación atrioventricular izquierda. En el momento de la consulta, estaba en tratamiento con pimobendán cada 12 horas, benaceprilo y espironolactona cada 24 horas, furosemida cada 12 horas y amiodarona cada 24 horas, esta última añadida recientemente por la presunta detección de arritmias supraventriculares.
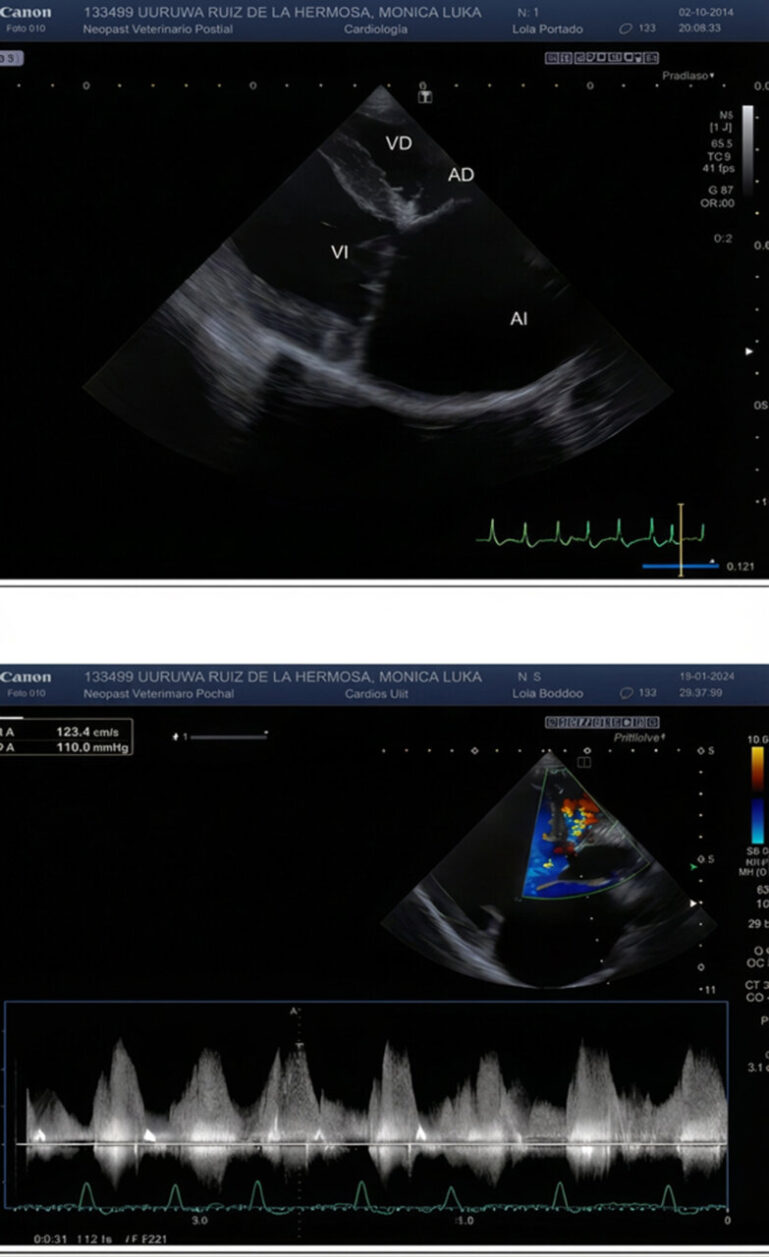
Antes de la planificación de la cirugía, se recomendó una revisión por parte del Servicio de Cardiología del centro para evaluar la gravedad de la patología cardiaca. Se realizó un estudio ecocardiográfico, que mostró la existencia de un defecto perimembranoso del septo interventricular y cuadricuspidía aórtica con grave remodelación atrioventricular izquierda y complicada con fibrilación atrial (FA) (imágenes 1 y 2). Se decidió mantener el tratamiento actual, con la excepción de la amiodarona, que se suspendió y sustituyó por diltiazem cada 12 horas y digoxina cada 12 horas para el tratamiento de la FA. También se añadió amlodipino cada 12 horas.
Tras una interconsulta entre los servicios de Anestesia, Cardiología y Cirugía, se programó la intervención quirúrgica para la amputación de las falanges necrosadas. Se pautó un ayuno de 8 horas de sólidos y 2 horas de agua y se recomendó retirar el banaceprilo y el amlodipino 12 horas antes de la anestesia. La analítica sanguínea preanestésica no mostró ninguna anomalía.
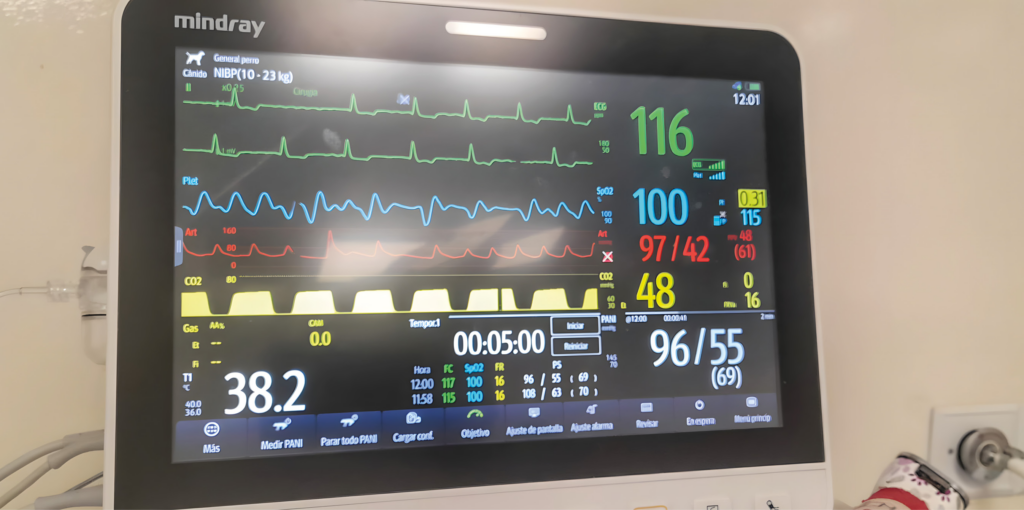
En la exploración física se apreció que el paciente estaba nervioso, aunque era manejable, y su condición corporal era de 5/9. La auscultación mostró un soplo cardiaco grado V/VI y ritmo cardiaco irregular a la auscultación debido a la FA, con frecuencia cardiaca (FC) 100-120 lpm. Se asignó al paciente una clasificación de riesgo anestésico ASA IV5.
Se realizó una premedicación anestésica con metadona 0,3 mg/kg intramuscular (IM), que produjo un grado de sedación leve pero suficiente para facilitar el manejo del paciente. Se cateterizó un acceso venoso en la vena cefálica derecha con cánula de 20 G, y tras preoxigenar al paciente durante 5 minutos, se realizó la inducción anestésica con propofol 6 mg/kg y midazolam 0,2 mg/kg. Se intubó con tubo de 8,5 mm y se inició el mantenimiento anestésico intravenoso con infusión intravenosa continua (IIC) de propofol (0,5-0,4 mg/kg/minuto) y dexmedetomidina 0,5 mcg/kg/h. Se cateterizó un acceso arterial en la arteria metatarsiana izquierda con cánula de 22G. Se administró fluidoterapia con Ringer Lactato a un máximo de 3 ml/kg/h (restando el volumen correspondiente a las IIC). Como analgesia adicional, se realizó un bloqueo en anillo con 4 mg/kg de lidocaína al 2 %. Como antibioterapia, se administró amikacina 20 mg/kg IVA.
Se administró un flujo de gas fresco con mezcla de oxígeno y aire al 50 %. Se inició la ventilación mecánica controlada por volumen, con el fin de garantizar normocapnia con los siguientes parámetros: volumen tidal (Vt) 10-12 ml/kg, frecuencia respiratoria (FR) 12-15 rpm, relación inspiración: espiración (I: E) de 1:2, pausa inspiratoria 30 %, presión positiva al final de la espiración (PEEP) aportada por la propia estación de anestesia (1-2 cmH2O), y presiones inspiratorias pico y meseta de 9-10 cm H2O.
Durante toda la anestesia se monitorizaron: electrocardiograma (ECG), saturación de oxígeno de la hemoglobina (SpO2), fracción espirada de dióxido de carbono (EtCO2), presiones arteriales sistólica (PAS), diastólica (PAD) y media (PAM) por medición no invasiva (oscilometría) e invasiva, temperatura, gases anestésicos, espirometría y plano anestésico mediante observación de reflejo palpebral y posición del globo ocular.
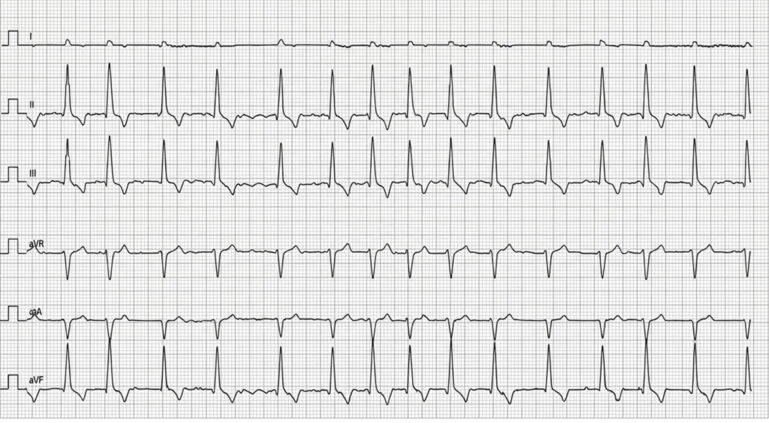
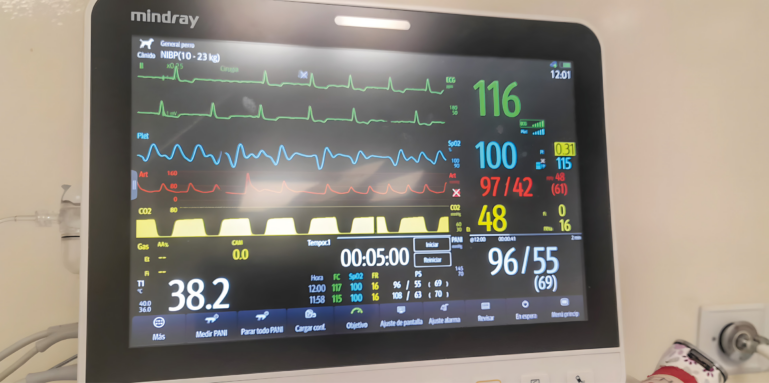
La duración total de la anestesia fue de 60 minutos y la de la cirugía, de 40 minutos. El electrocardiograma mostró un ritmo predominantemente de FA a 110-120 lpm, sin otras anomalías reseñables (imágenes 3 y 4). Tras la extubación, se administró meloxicam 0,2 mg/kg. El paciente se recuperó de forma lenta pero adecuada, sin que se observasen anomalías en la exploración física. Se mantuvo la oxigenoterapia por mascarilla en el posoperatorio temprano para evitar el riesgo de hipoxemia y se monitorizó la saturación de oxígeno mientras el paciente lo toleró. Fue dado de alta el mismo día por la tarde.
Discusión
En el caso descrito, se consiguió realizar un manejo anestésico seguro en un paciente con enfermedad cardiaca avanzada, gracias al conocimiento tanto de la fisiopatología de dicha enfermedad como de los factores que podrían empeorarla durante la anestesia. Es importante destacar también la excelente comunicación entre los tres servicios implicados (Anestesia, Cardiología y Cirugía), lo cual siempre es clave en el manejo de pacientes con elevado riesgo anestésico6.
Los pacientes con patología cardiaca presentan un descenso del gasto cardiaco (GC) en mayor o menor medida, lo que a la larga reduce la presión arterial (PA)2. La mayoría de los fármacos empleados en anestesia afectan al GC de diferentes formas, por lo que es importante saber cuáles están indicados y cuáles deben evitarse en función de la patología y su gravedad.
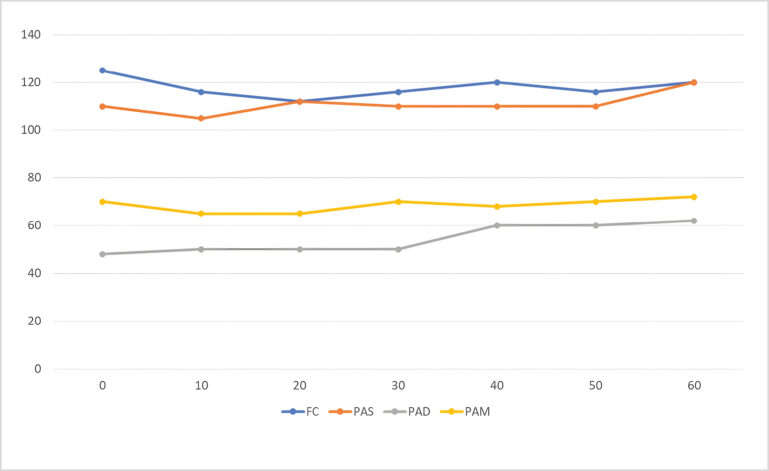
En los pacientes con DSIV, el objetivo fundamental durante la anestesia es evitar que se produzca una reversión del flujo a derecha-izquierda, para lo cual deben evitarse descensos en la resistencia vascular sistémica (RVS) y/o aumentos en la resistencia vascular pulmonar (RVP)4,6. El paciente de este caso presentaba, además, una dilatación de cámaras cardiacas grave y FA, por lo que también se requería evitar una sobrecarga de fluidos y una mayor reducción del GC, que ya estaba de por sí comprometido (tabla 1).
| Tabla 1. Resumen de las principales consideraciones anestésicas en el manejo de este paciente. | |
| ¿Qué debemos evitar? | Pautas para conseguirlo |
| Aumento de la RVP | Evitar acidosis e hipercapnia: emplear ventilación mecánica.
Evitar hipoxemia: preoxigenación, evitar apnea en la inducción, mantener oxígeno en la recuperación anestésica. Evitar presiones ventilatorias elevadas. |
| Descenso de la RVS | Evitar fármacos con efecto vasodilatador: acepromacina.
Mantenimiento anestésico intravenoso preferible al inhalatorio. Uso de IIC de dexmedetomidina en dosis baja. |
| Descenso del GC | Mantener FC similar a la basal o un poco más elevada.
Mantener volumen sistólico: asegurar aporte de fluidos. Evitar uso de dexmedetomidina en bolos (mayor impacto sobre el GC). |
| Sobrecarga de fluidos | Fluidoterapia con un máximo de 3 ml/kg/h (descontando velocidad de la anestesia total intravenosa). |
Se retiró la pauta de administración de benaceprilo y amlodipino 12 horas antes de la anestesia para evitar el desarrollo de hipotensión asociada al descenso de la RVS. Aunque no existe todavía un consenso a este respecto, las guías de anestesia y monitorización más recientes en pequeños animales recomiendan no administrar fármacos antihipertensivos el día de la anestesia7.
Se optó por premedicación con metadona, ya que proporciona analgesia de cara a la cirugía, sedación y reducción de los requerimientos de anestésicos generales, con efectos cardiovasculares mínimos5,6,8. Se decidió emplear la vía IM para minimizar el estrés por la manipulación, lo que es esencial en pacientes con patología cardiaca2,6. La sedación proporcionada fue leve, pero suficiente para poder cateterizar un acceso venoso en el paciente. Se descartó el uso en premedicación de agonistas adrenérgicos α-2 para evitar un descenso del GC, y de acepromacina para evitar una reducción de la RVS4,6.
La preoxigenación es esencial en cualquier paciente antes de la inducción anestésica para minimizar el riesgo de hipoxemia por hipoventilación o apnea7. En este caso, evitar la hipoxemia era todavía más importante, puesto que esta podría aumentar la vasoconstricción pulmonar hipóxica (VPH), lo que incrementaría la RVP2,4.
Para la inducción anestésica se empleó propofol en combinación con midazolam. La inducción proporcionada por el propofol es rápida, suave y, por lo general, segura si se realiza de forma lenta y con dosis-efecto; se considera adecuada en pacientes con patologías cardiacas como esta6,9. Se optó por una coinducción con midazolam con el fin de reducir los requerimientos de propofol10,11, dado que el grado de sedación conseguido con la premedicación había sido leve.
Se decidió realizar un mantenimiento anestésico con IIC de propofol en lugar de mantenimiento inhalatorio por varias razones:
- En primer lugar, la anestesia total intravenosa (TIVA) ha mostrado una mayor estabilidad cardiovascular y mejor mantenimiento de la presión arterial sistémica que la anestesia inhalatoria12,13.
- En segundo lugar, el propofol parece tener mínimos efectos sobre la RVP incluso con dosis elevadas14. Aunque en medicina humana se ha descrito que el propofol puede favorecer la reversión del flujo a derecha-izquierda por descenso de la RVS15, dicho descenso es transitorio y dosis-dependiente.
El mantenimiento con IIC de alfaxalona hubiera sido una buena alternativa, ya que ha demostrado también una excelente estabilidad cardiovascular16, pero también ha demostrado producir recuperaciones lentas y de muy mala calidad en perros16,17.
Con la adición de IIC de dexmedetomidina en dosis bajas se buscaban varios objetivos: reducir los requerimientos de propofol18, producir un aumento de la RVS con mínimos efectos sobre el GC19, proporcionar analgesia adicional20 y favorecer una recuperación tranquila21.
Dada la remodelación cardiaca por dilatación cameral que presentaba el paciente, se optó por una fluidoterapia conservadora con un máximo de 3 ml/kg/h de Ringer Lactato22, volumen que se ajustó en función de las velocidades de administración de las IIC de propofol y dexmedetomidina.
Se aplicó ventilación mecánica desde la intubación para minimizar el riesgo de acidosis respiratoria e hipercapnia, las cuales producen un aumento de la RVP4. Se evitaron presiones inspiratorias elevadas y solo se utilizó el valor de PEEP proporcionada por la propia estación de anestesia, con el mismo fin4.
Durante la recuperación anestésica, un elevado porcentaje de pacientes tienden a presentar hipoxemia, por lo que se monitorizó la SpO2 en el posoperatorio temprano y se administró aporte de oxígeno a través de mascarilla4,6 mientras el paciente toleró ambas cosas.
En el momento de la anestesia, el paciente presentaba FA, probablemente asociada a la grave dilatación auricular. Por lo general, dado que la contracción auricular solo contribuye en un 20 % al llenado ventricular, la existencia de FA en un paciente no suele comprometer el GC de forma significativa, tal y como ocurrió en este paciente4. El tratamiento previo con diltiazem y digoxina y la administración de metadona con el consecuente aumento de tono vagal probablemente permitieron un buen control de la FC a pesar de la FA4,20. El empleo de IIC de dexmedetomidina pudo tener también un efecto beneficioso. Los agonistas adrenérgicos α-2 protegen el miocardio de potenciales arritmias al aumentar el tono vagal por su acción sobre receptores adrenérgicos4,20, y porque evitan la aparición de focos isquémicos gracias al agonismo debido a su acción sobre receptores imidazólicos20,23.
Conclusiones
El manejo anestésico de un paciente con enfermedad cardiaca, especialmente si es avanzada, implica un conocimiento en profundidad de la fisiopatología de dicha enfermedad y de los potenciales efectos que los fármacos anestésicos puedan tener en el paciente. Es esencial una revisión por un cardiólogo especialista, así como una adecuada comunicación entre servicios para modificar el tratamiento médico del paciente y planificar la anestesia de la forma más segura posible.
Bibliografía:
- Redondo-García JI et al. Mortalidad anestésica en gatos en España. Resultados del proyecto COMPLRED. Clin Vet Peq Anim, 2023; 43 (4): 247-260
- Martinez-Albiñana, A., Plaza-Del Castaño, Q., Aguilar-Gallego, N., Fernandez-Rodriguez, P., & Viscasillas-Monteagudo, J. (n.d.). Manejo anestésico del paciente con patología cardiaca adquirida. Clin Vet Peq Anim, 2020; 42 (3): 169 – 179
- Van de Watering, A., & Szatmári, V. Spontaneous closure of an isolated congenital perimembranous ventricular septal defect in two dogs. BMC Veterinary Research, 2022. 18(1).
- Duke-Novakovsky T, De Vries M, Seymour C. BSAVA Manual of canine and feline anesthesia and analgesia, 3th edition.2016.
- Oliveira, P., Domenech, O., Silva, J., Vannini, S., Bussadori, R., & Bussadori, C. Retrospective review of congenital heart disease in 976 dogs. Journal of Veterinary Internal Medicine, 2011. 25(3), 477–483.
- Lamont L, Grimm K, Robertson S, Love L, Schroeder C. Veterinary anaesthesia and analgesia. The sixth edition of Lumb & Jones. 2024. Ed. Willey Blackwell.
- Grubb T, Sager J, Gaynor JS, Montgomery E, Parker JA, Shafford H, Tearney C. 2020 AAHA Anesthesia and Monitoring Guidelines for Dogs and Cats. J Am Anim Hosp Assoc. 2020 Mar/Apr;56(2):59-82.
- Bradbrook CA, Clark L. State of the art analgesia- recent developments in pharmacological approaches to acute pain management in dogs and cats. Part 1. Vet J. 2018; 238:76-82.
- Gimenes AM, de Araujo Aguiar AJ, Perri SHV, et al. Effect of intravenous propofol and remifentanil on heart rate, blood pressure and nociceptive response in acepromazine premedicated dogs. Vet Anaesth Analg 2011; 38: 54–62
- Minghella E, Auckburally A, Pawson P, Scott ME, Flaherty D. Clinical effects of midazolam or lidocaine co-induction with a propofol target-controlled infusion (TCI) in dogs. Vet Anaesth Analg. 2016 Sep;43(5):472-81.
- Aguilera R, Sinclair M, Valverde A, Bateman S, Hanna B. Dose and cardiopulmonary effects of propofol alone or with midazolam for induction of anesthesia in critically ill dogs. et Anaesth Analg. 2020 Jul;47(4):472-480.
- Bustamante R, Aguado D, Cediel R, Gómez de Segura IA, Canfrán S. Clinical comparison of the effects of isoflurane or propofol anaesthesia on mean arterial blood pressure and ventilation in dogs undergoing orthopaedic surgery recei – ving epidural anaesthesia. Vet J. 2018. 233:49-54.
- Raffe, M. R. Total Intravenous Anesthesia for the Small Animal Critical Patient. Veterinary Clinics of North America – Small Animal Practice 2020. Vol. 50, Issue 6, pp. 1433–1444). W.B. Saunders.
- Naeije, R., Lejeune, P., Leeman, M., Melot, C., & Deloof, T. Effects of propofol on pulmonary and systemic arterial pressure-flow relationships in hyperoxic and hypoxic dogs Downloaded from. In Br. J. Anaesth 1989. (Vol. 62).
- Williams GD, Jones TK, Hanson KA, et al. The hemodynamic effects of propofol in children with congenital heart disease. Anesth Analg 1999; 89: 1411–1416.
- Dehuisser V, Bosmans T, Devreese M, Gehring R, Croubles S, Duchateu L, Polis I. Alfaxalone total intravenous anaesthesia in dogs: pharmaco – kinetics, cardiovascular data and recovery charac – teristics. Vet Anaesth Analg. 2019. 46(5):605-612. roceedings IVECCS. 2019: 25-28.
- Suarez MA, Dzikiti BT, Stegmann FG, Hartman M. Comparison of alfaxalone and propofol administered as total intravenous anaesthesia for ovariohysterectomy in dogs. Vet. Anaesth. Analg. 2012. 39: 236-244.
- Smith CK, Seddighi R, Cox SK, Sun X, Knych HK, Doherty TJ. Effect of dexmedetomidine on the minimum infusion rate of propofol preventing movement in dogs. Vet Anaesth Analg. 2017 Nov;44(6):1287-1295
- Martín-Flores M, Moy-Trigilio K E, Campoy L, Araos J. The use of dexmedetomidine during pulmonic balloon valvuloplasty in dogs. Vet Rec. 2021 Jun;188(11)
- Dugdale AHA, Beaumont G, Bradbrook C, Gurney M. Veterinary anaesthesia: principles to practice. 2nd edition. 2020. Ed. Willey Blackwell
- Jarosinski, S. K., Simon, B. T., Baetge, C. L., Parry, S., & Araos, J. The Effects of Prophylactic Dexmedetomidine Administration on General Anesthesia Recovery Quality in Healthy Dogs Anesthetized With Sevoflurane and a Fentanyl Constant Rate Infusion Undergoing Elective Orthopedic Procedures. Frontiers in Veterinary Science, 2021. 8
- Pardo M.; Spencer E.; Odunayo A.; Ramirez M.L.; Rudolf E.; Shafford H.; Weil A.; Wolff E.; 2024 AAHA Fluid Therapy Guidelines for Dogs and Cats 2024
- Roekaerts, P. M. H. J., Prinzen, F. W., & de Lange, S. Beneficial effects of dexmedetomidine on ischaemic myocardium of anaesthetized dogs. British Journal of Anaesthesia, 1996. 77(3), 427–429.